
- 作者:lily-cha 数据来源:米内网 点击数: 更新时间:6/28/2013

2013年3月百健艾迪的重磅口服抗MS药无富马酸二甲酯(TECFIDERA)获得FDA批准,用于治疗成人复发型多发硬化症。TECFIDERA成功获批的消息以公布,其公司股价上涨3.2%,创下自1991年9月IPO以来最高收盘记录。有机构预测,到2017年TECFIDERA将为公司每年贡献32.5亿美元。
其实在产品的梯队方面,百健艾迪早已布局,2004年11月FDA批准了治疗MS的单抗药TYSABRI(那他珠单抗),它是FDA批准的第六个MS治疗药。那他珠单抗是一种合成的选择性粘附分子抑制剂,能与白细胞表面的a4联脂结合,阻止后者与粘附分子相互作用,抑制白细胞向炎症区域趋化,减轻炎症反应。那他珠单抗可用于对一线疾病缓解治疗(DMT)反应不佳或不耐受的复发性多发性硬化的治疗;亦用于既往未经治疗的侵袭性始发多发性硬化的治疗。那他珠单抗治疗MS功效强大,可以将疾病的复发率降低大约70%。虽然05年该产品出现过一些波折,但08年它又获得FDA批准的一个新的适应症,用于中重度活动性克罗恩(Crohn)病。在业绩销售方面,08年那他珠单抗有一个大的飞跃后,2011年终于成为年销售十亿美元俱乐部会员。基于对该药的后市看好,今年初公司宣布,以32.5亿美元从Elan公司手上获得Tysabri另外50%的股份,从而彻底拥有该药物。
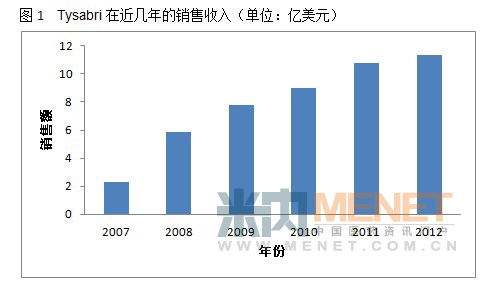
2011年,百健艾迪的Fampyra(氨吡啶)在欧洲获批并成功在澳大利亚、丹麦、德国、挪威和英国推出。该产品是从Acorda Therapeutics公司获得授权在美国市场外开拓和商业化的品种,而在美国市场,Acorda公司则以AMPYRA(达方吡啶)的商品名进行运作。Fampyra是帮助多发性硬化成年患者行走的一种药物。在众多MS患者中有64%~85%的人行走困难,约70%的患者认为行走困难是该疾病最为恼人的症状。而在多发性硬化病诊出后15年内,50%患者行走常需辅助器械;在疾病晚期,高达1/3的患者将不能行走。Fampyra正是解决患者的这一症状,它能加强受损伤神经的传导,是第1个用来恢复慢性脊髓损伤(SCI)患者一些神经学功能的化合物。它能通过阻滞无髓鞘神经轴突暴露的钾通道而恢复神经传导功能。Fampyra一经上市,就显示了超强的吸金能力。获批当年就录得一千四百万美元的销售,2012年更是达到了五千七百万美元,增长速度惊人。
鉴于目前多数治疗MS的药物剂型为注射剂,而对患者来说较为便利的给药途径还是口服制剂,于是百健艾迪追随诺华和赛诺菲的研究策略,开发了口服给药的TECFIDERA,研究显示,如果一天服药两次或三次,可使每年的复发率减少49%。该药的副作用与安慰剂类似,最常见的不良反应是脸红和影响胃肠道,而这些副作用可能会随时间推移而降低。正是由于良好的临床试验结果,众多机构分析师给出了未来市场美好的预期,TECFIDERA有机会成为百健艾迪公司的下一个重磅炸弹。
2013年5月21日百健艾迪宣布,已向FDA提交了PLEGRIDY(聚乙二醇化干扰素β-1a)的生物制剂许可申请(BLA),该药是一种聚乙二醇化皮下注射药物,用于复发型多发性硬化症的治疗。PLEGRIDY是一种新的分子实体,利用聚乙二醇化技术来延长干扰素β-1a(Avonex)的半衰期,延长其在体内的循环时间,能够减少用药次数。有理由相信随着PLEGRIDY的批准将进一步增强百健艾迪本来就已强大的MS药物产品组合。
在我国上市的MS治疗药基本为干扰素类,而且为进口产品。百健艾迪的MS产品只有Avonex向CFDA进行了申报。由于生物仿制药拥有大型、复杂的分子结构,这就决定了这类药物要求长期和昂贵的研发费用,而将其商业化同样具有挑战性,这注定了国内企业在决定开发此类产品时抱有的谨慎心理。除治疗癌症等的单抗类药物国内企业有涉猎外,其他免疫性疾病的单抗药物基本是外企在角逐市场。值得欣慰的是北京天坛生物09年以7类新药进行了注射用重组人干扰素β-1b的申报,而北京福瑞康正医药今年以3.1类化药进行达方吡啶原料药及缓释片的申报,正式宣布进入MS治疗药物的探索性尝试。
| ・ | 高端医疗人才供需错配 多点执业效果存疑 | 6月28日 |
| ・ | 专家痛批中国医改五大误判 医改未入深水区 | 6月26日 |
| ・ | 三类医保或难在本月底前如期归并管理 | 6月25日 |
| ・ | 药品管理法将大修 缩短新药审批时限 | 6月24日 |
| ・ | 香港通报批次银翘片未检出非法添加 | 6月20日 |
| ・ | 国家卫生计生委职能确立 主任一正四副 | 6月19日 |
| ・ | 逐步缓解群众看病难看病贵问题 | 6月18日 |
| ・ | 最严食品安全法年内完成修订 如何重典治乱 | 6月17日 |
| ・ | 食品安全法近期修订 将设最严格监管问责制 | 6月14日 |
| ・ | 刘延东:实施好医保医疗医药“三医联动” | 6月13日 |
| ・ | 国际医药互联月刊2013(6) | 6月25日 |
| ・ | GMP认证数据库下载 | 5月30日 |
| ・ | 国际医药互联月刊2013(5) | 5月22日 |
| ・ | GSP认证数据库下载 | 5月20日 |
| ・ | 中药保护品种数据库下载 | 5月15日 |
| ・ | 国家药监局新药报批数据库下载 | 5月6日 |
| ・ | 国际医药互联月刊2013(4) | 4月25日 |
| ・ | 国际医药互联月刊2013(5) | 5月22日 |
| ・ | 国际医药互联月刊2013(4) | 4月25日 |
| ・ | 国际医药互联月刊2013(3) | 4月1日 |
| ・ | 国际医药互联月刊2013(2) | 4月1日 |
| ・ | 国际医药互联月刊2013(1) | 1月23日 |
| ・ | 国际医药互联月刊2012(12) | 12月21日 |
| ・ | 国际医药互联月刊2012(11) | 12月10日 |
| ・ | 三种祛痰药华源市场分析 | 12月21日 |
| ・ | 百合固金丸华源市场分析 | 8月9日 |
| ・ | 柏子养心丸华源市场分析 | 8月3日 |
| ・ | 白癜风胶囊华源市场分析 | 8月2日 |
| ・ | 八珍益母丸华源市场分析 | 7月30日 |
| ・ | 阿司匹林肠溶片华源市场分析 | 7月9日 |
| ・ | 硝酸益康唑栓华源市场分析 | 5月14日 |